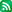

중국 화장품 수출의 성패는 이 세 가지를 이해하는 것에서 시작합니다.
규제 기관: NMPA (국가약품감독관리국) - 한국의 식약처에 해당하며, 모든 화장품의 허가 및 등록을 총괄하는 막강한 기관입니다.
핵심 개념 1: 제품 분류 (특수 vs 일반)
특수화장품 (Special Cosmetics): 염모, 펌, 기미제거/미백, 자외선차단, 탈모방지, 신규 효능 선전 제품. (총 5+a종) -> [허가제] 절차가 매우 복잡하고 오래 걸림.
일반화장품 (General Cosmetics): 특수화장품을 제외한 나머지 (기초 스킨케어, 메이크업, 향수, 헤어케어 등). -> [등록제(비안)] 상대적으로 빠름.
핵심 개념 2: 경내책임인 (Domestic Responsible Agent)
필수: 해외 제조사는 반드시 중국 내에 법적 책임을 지는 기업(경내책임인)을 지정해야 합니다.
역할: 제품의 품질 및 안전성 책임, NMPA 소통, 리콜, 부작용 보고 등 막중한 법적 의무를 집니다. (단순 수입상보다 훨씬 무거운 책임)
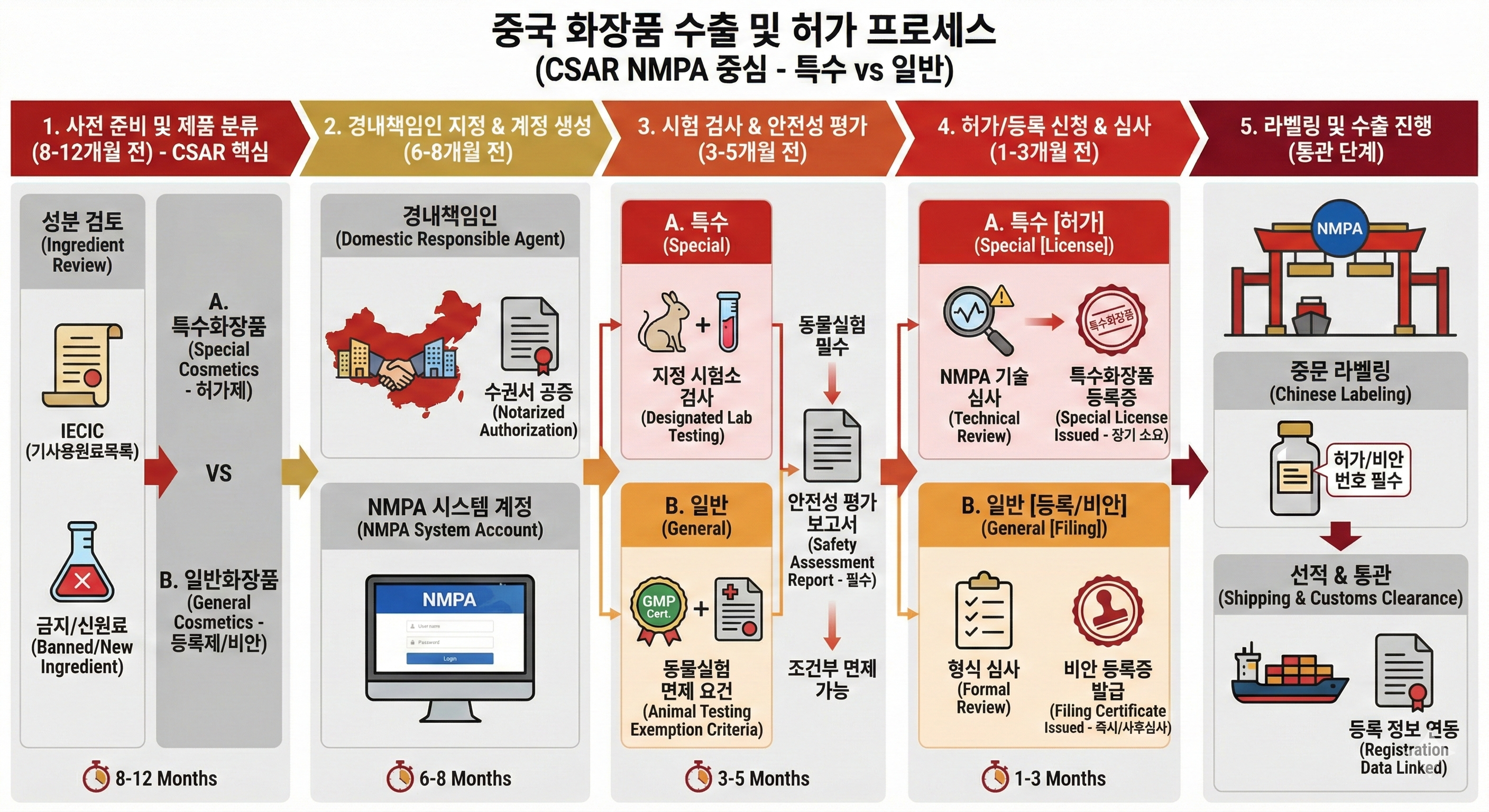
1단계: 사전 준비 및 제품 분류 (수출 8~12개월 전)
가장 기초적이면서도 중요한 단계입니다. 내 제품이 중국 법규상 어디에 속하는지 판단해야 합니다.
1-1. 성분 검토 (IECIC 및 사용금지 원료)
기사용화장품원료목록(IECIC): 중국에 이미 등록된 원료(약 8,900여 종) 목록에 내 제품의 모든 성분이 포함되어 있는지 확인합니다.
신원료: IECIC에 없는 원료를 사용했다면 '신원료 등록/허가'를 먼저 받아야 하는데, 이는 화장품 등록보다 더 어렵고 비용이 많이 듭니다. (가급적 IECIC 내 원료 사용 권장)
금지/제한 성분: 중국 화장품 안전기술규범에 따른 금지 및 사용 한도 성분을 철저히 검토해야 합니다.
1-2. 제품 분류 확정 (특수 vs 일반)
제품의 효능 클레임과 성분을 바탕으로 '특수'인지 '일반'인지 확정합니다. 이 분류에 따라 이후의 모든 타임라인과 비용이 결정됩니다.
2단계: 경내책임인 지정 및 시스템 계정 발급 (수출 6~8개월 전)
중국 현지 파트너와 법적 계약을 맺고 NMPA 시스템에 접속할 권한을 얻는 단계입니다.
2-1. 경내책임인 선정 및 수권서 공증
신뢰할 수 있는 경내책임인을 선정하여 '수권서(위임장)'를 작성하고, 한국 내에서 공증 및 영사 인증을 받습니다.
2-2. NMPA 시스템 계정 개설
경내책임인이 NMPA 화장품 등록 비안 정보 서비스 플랫폼에 기업 정보를 등록하고 계정을 개설합니다. 이후 모든 서류 제출은 이 시스템을 통해 전자적으로 이루어집니다.
3단계: 시험 검사 및 안전성 평가 (수출 3~5개월 전)
중국 정부가 인정한 시험소에서 제품 테스트를 진행하고, 안전성 평가 보고서를 작성하는 단계입니다.
3-1. NMPA 지정 시험소 검사
중국 내 지정된 시험 기관에 샘플을 보내 미생물, 이화학, 독성학, 인체 안전성 및 효능 평가(특수화장품 필수) 시험을 진행합니다.
3-2. 동물실험 면제 요건 확인 (일반화장품 한정)
조건부 면제: 2021년부터 '일반화장품'에 한해 다음 두 조건을 모두 만족하면 동물실험이 면제될 수 있습니다.
제조국(한국) 정부가 발급한 GMP 인증서 (또는 이에 준하는 품질관리시스템 인증서) 제출.
충분한 데이터를 바탕으로 한 제품 안전성 평가 보고서 제출 및 확인.
예외: 영유아/아동용 제품, 신원료 사용 제품, 경내책임인이 중점 감시 대상인 경우는 면제 불가.
3-3. 안전성 평가 보고서 작성 (필수)
화장품감독관리조례(CSAR) 시행으로 가장 강화된 부분입니다. 원료 및 완제품의 안전성을 입증하는 전문적인 평가 보고서를 반드시 작성하여 제출해야 합니다.
4단계: 허가/등록 신청 및 서류 제출 (수출 1~3개월 전)
준비된 모든 자료를 NMPA 시스템에 업로드하여 심사를 받는 단계입니다.
4-1. 서류 접수 (Dossier Submission)
경내책임인이 시스템을 통해 신청서, 제품 배합표, 제조공정표, 품질표준, 시험성적서, 안전성 평가 보고서, 라벨 디자인 등을 제출합니다.
4-2. 심사 (기술 심사 vs 형식 심사)
특수화장품 [허가]: NMPA의 엄격한 '기술 심사'를 거칩니다. 보완 요구가 빈번하며 통상 6개월~1년 이상 소요됩니다. 합격 시 '특수화장품 등록증(허가증)'이 발급됩니다.
일반화장품 [등록(비안)]: 형식 요건을 갖추면 자료 제출 즉시 '등록 완료 증명(비안등록증)'이 발급되고 시스템에 공개됩니다. (통상 1~3개월). 단, 등록 후 3개월 이내에 NMPA가 사후 기술 심사를 진행하며, 문제 발견 시 등록이 취소될 수 있습니다.
5단계: 라벨링 및 수출 진행 (통관 단계)
허가/등록이 완료된 후 실제 제품에 중문 라벨을 부착하고 수출하는 단계입니다.
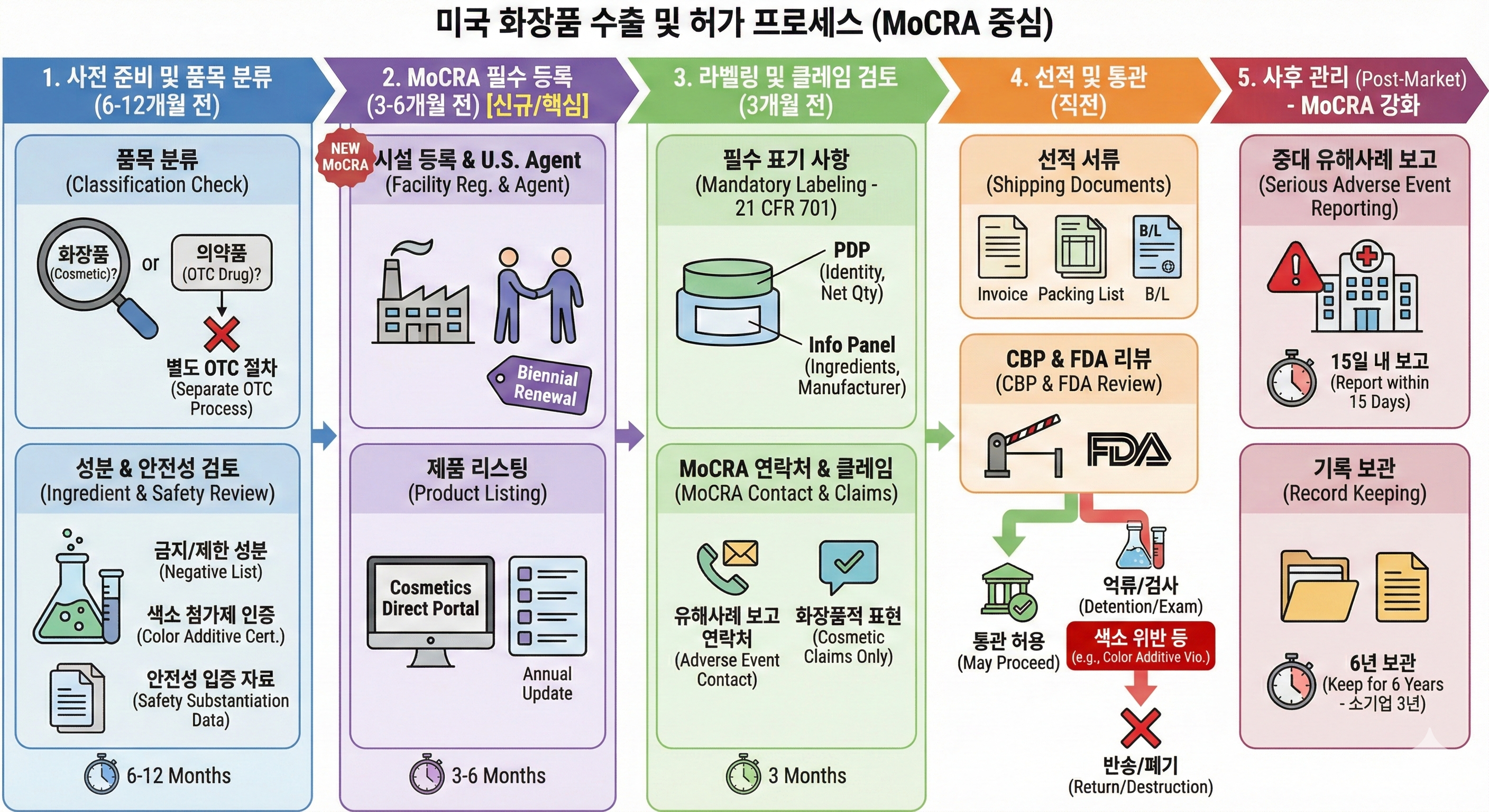
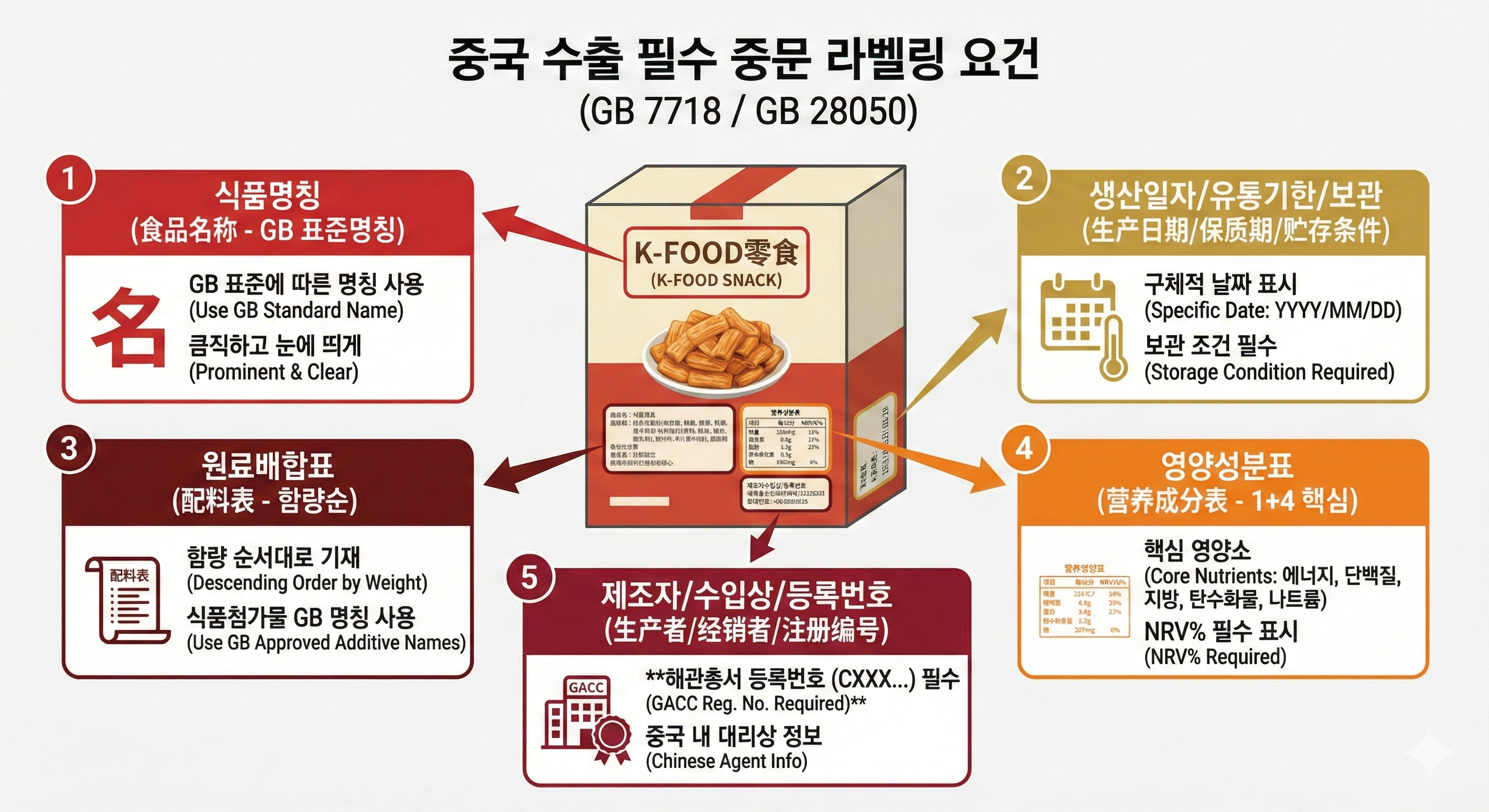
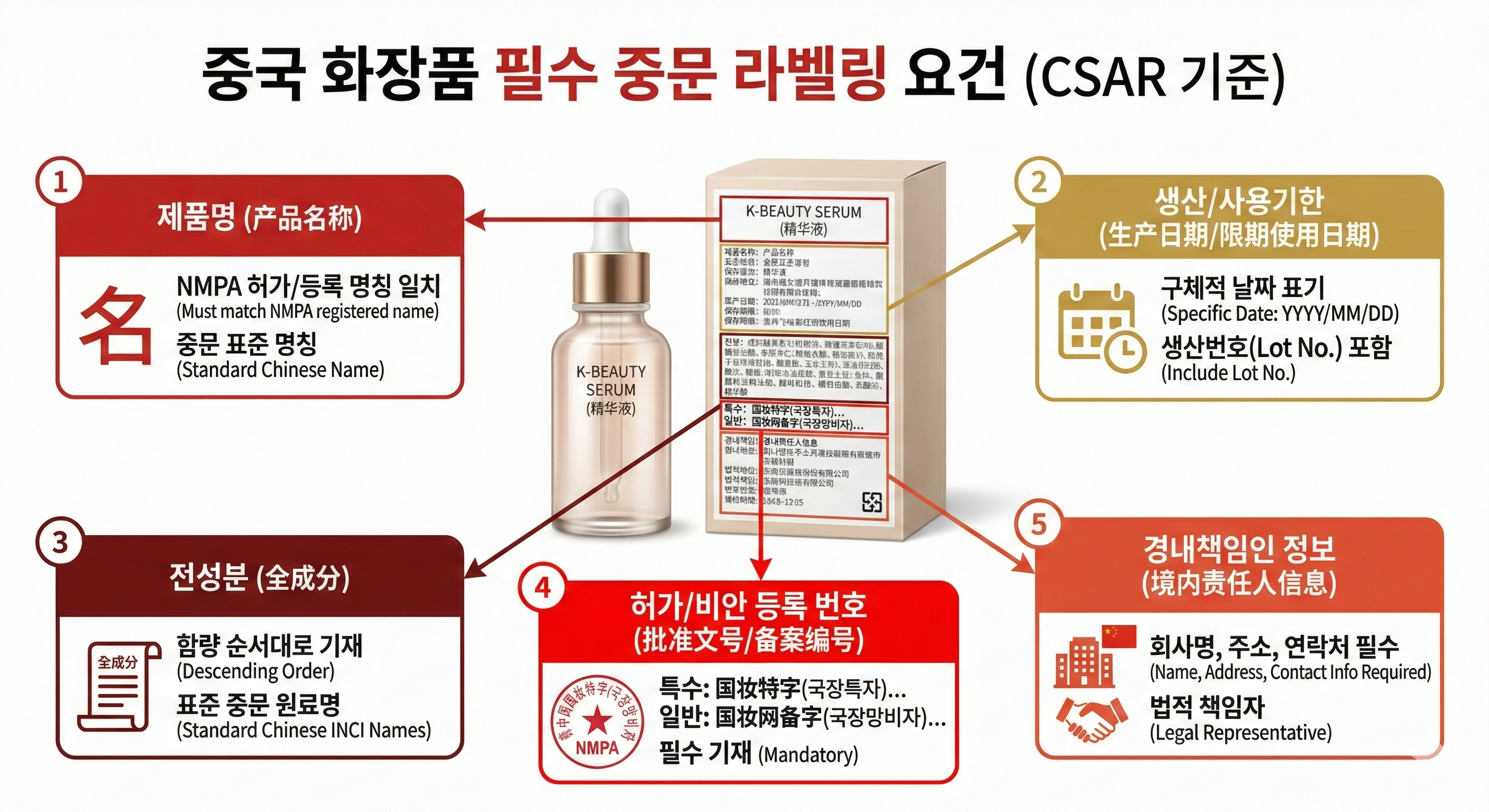
5-1. 중문 라벨링 (GB 5296.3 등)
제품에 직접 인쇄하거나 견고한 스티커 형태로 부착해야 합니다.
필수 표시: 제품 중문명, 전성분, 순함량, 제조사/경내책임인 명칭 및 주소, 생산번호/사용기한, 허가/비안 등록 번호, 안전 경고 문구 등.
5-2. 선적 및 통관
허가/등록증 사본, 경내책임인 정보 등을 첨부하여 수출 신고를 진행합니다. 중국 세관은 NMPA 시스템과 연동되어 등록 정보를 확인 후 통관을 허용합니다.
와이에스엠경영컨설팅 윤수만 소장 (화장품 해외마케팅/수출 강사)