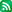1. 미국 FDA 화장품 제조시설 등록 절차 가이드
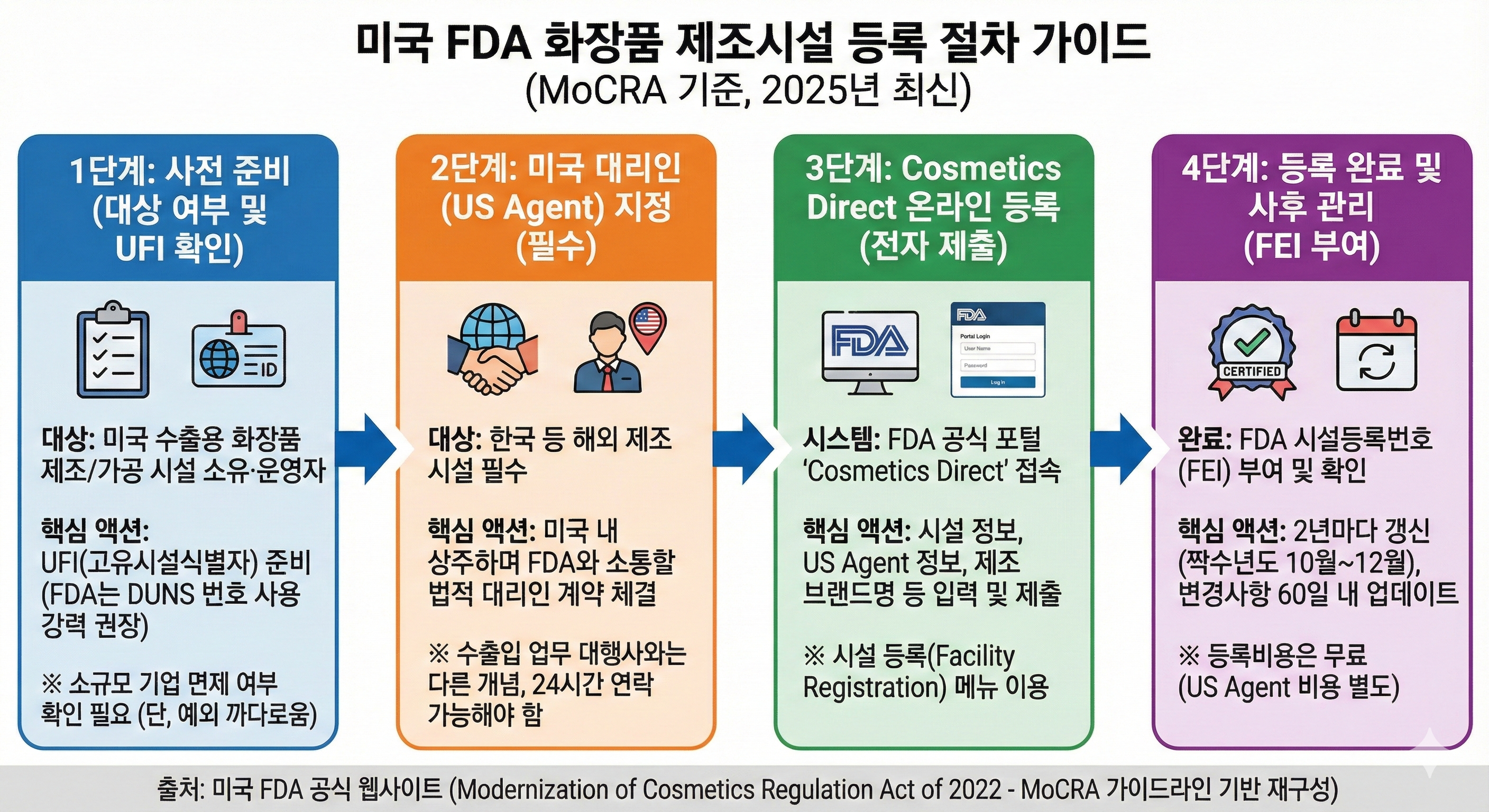
2. 미국 FDA 해외(한국) 화장품 제조소 실사 프로세스
도표 단계FDA 공식 근거 및 용어설명
1단계: 사전 통지FDA Form 482 (Notice of Inspection)FDA가 조사를 나갈 때 발행하는 법적 통지서입니다. 해외 실사의 경우 비자 발급, 일정 조율 등을 위해 통상적으로 미리 연락(Pre-announcement)을 취합니다. (근거: FD&C Act Section 704)
2단계: 현장 실사cGMP & Data IntegrityMoCRA는 FDA에게 화장품 GMP 규정을 만들도록 지시했습니다. 심사관들은 현장에서 제조 기록이 조작되지 않았는지(데이터 무결성)를 현미경처럼 들여다봅니다.
3단계: Form 483 발부FDA Form 483 (Inspectional Observations)실사 마지막 날, 심사관이 발견한 '법규 위반 의심 사항'을 적어서 공장 책임자에게 주는 공식 문서입니다. (FDA 실사의 꽃(?)이라고 불립니다.)
4단계: 15일 내 대응RPM (Regulatory Procedures Manual)FDA의 내부 규제 절차 매뉴얼(RPM)에 따르면, 기업이 Form 483 수령 후 영업일 기준 15일 이내에 적절한 답변을 보내면, 경고장 발송 전에 이를 참작해 줍니다. (매우 중요한 실무 룰입니다.)
5단계: 후폭풍Warning Letter & Import Alert답변이 부실하면 공식 경고장(Warning Letter)이 날아오고, 해외 공장의 경우 최악의 조치인 '수입 경보(Import Alert)' 리스트에 올려버립니다. 이렇게 되면 제품이 미국 항구에서 자동 억류됩니다.
와이에스엠경영컨설팅 윤수만 소장