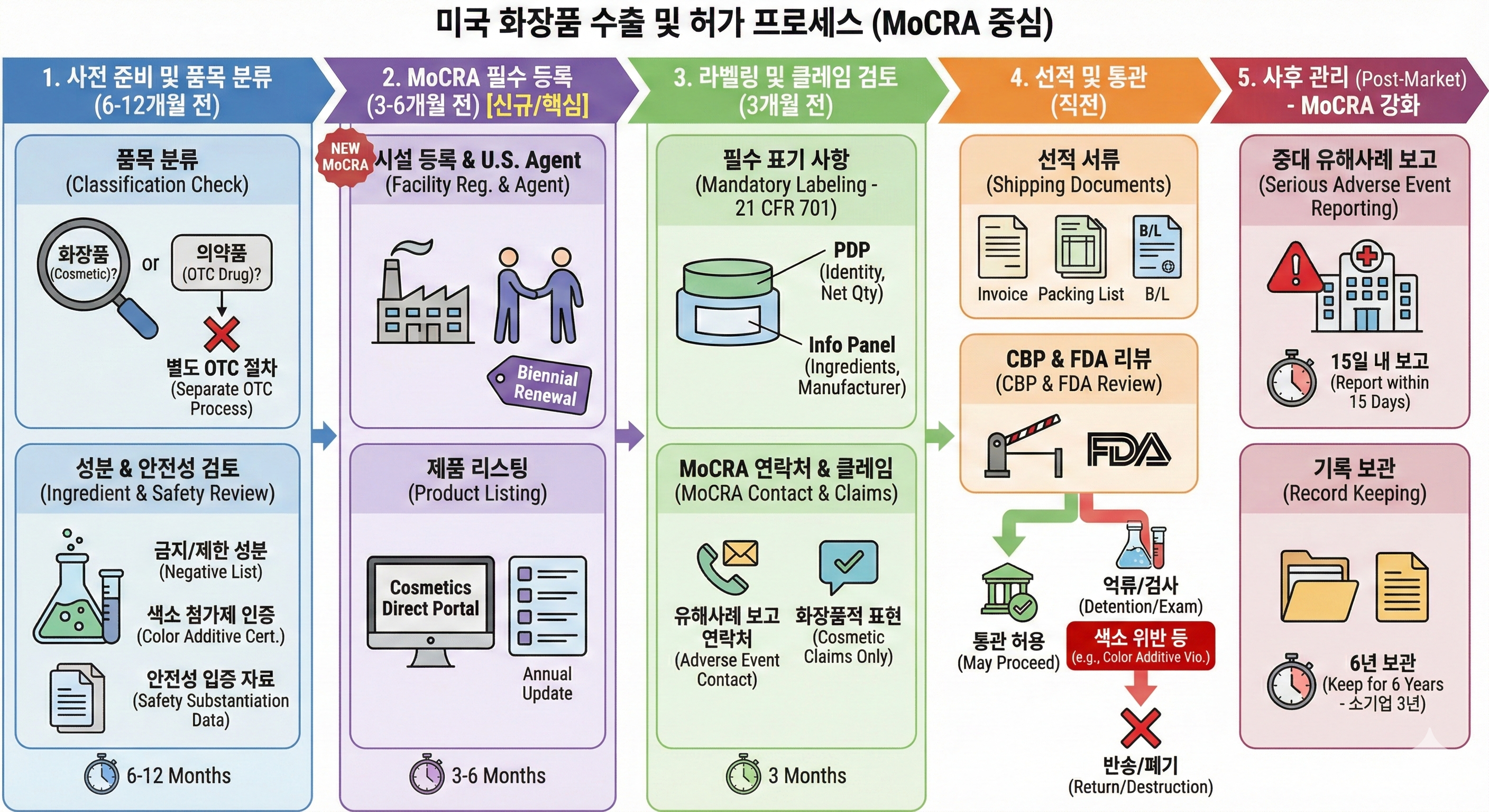
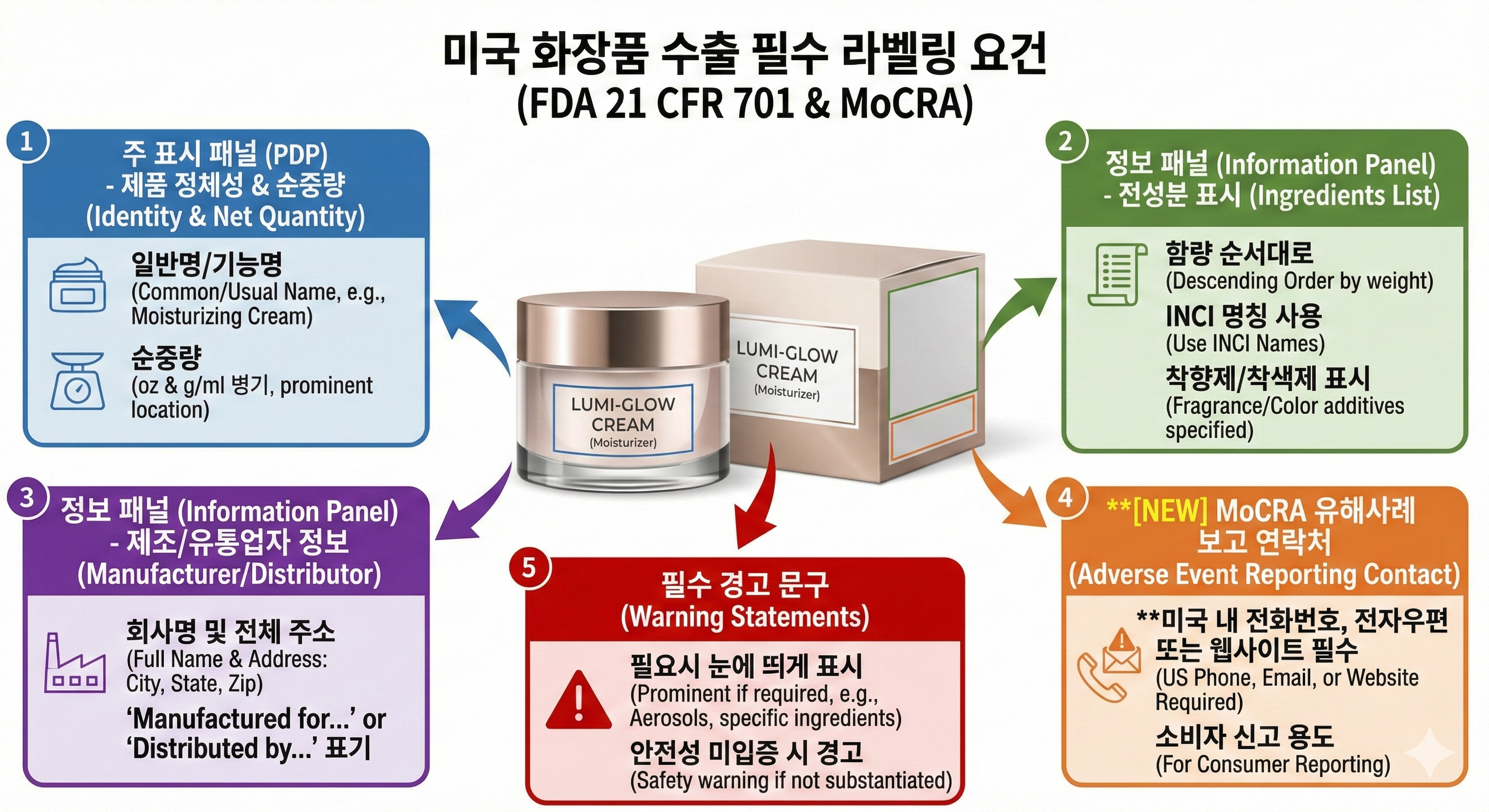
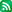2025년 현재 미국은 K뷰티의 가장 큰 수출국입니다. 그런데 미국 화장품 규제가 80년 만에 전면 개정됐습니다. 2022년 MoCRA(화장품 현대화법)가 시행되면서 시설 등록 의무, 이상반응 보고, FDA 강제 리콜 권한이 새로 생겼습니다. 더 큰 문제는 연방 FDA를 통과해도 끝이 아니라는 점입니다. 캘리포니아·뉴욕·워싱턴·버몬트 등 17개 이상의 주가 연방보다 훨씬 엄격한 자체 규제를 시행하고 있습니다. 아마존 미국에서 팔리는 제품은 캘리포니아 기준을 충족해야 합니다. 이 자료는 MoCRA의 핵심 변화, 연방 vs 주 규제 2중 구조, K뷰티가 미국에서 새롭게 막히는 4가지 구조를 정리했습니다.
무료② — 한국 허용 but 미국에서 막히는 원료 사례 7가지
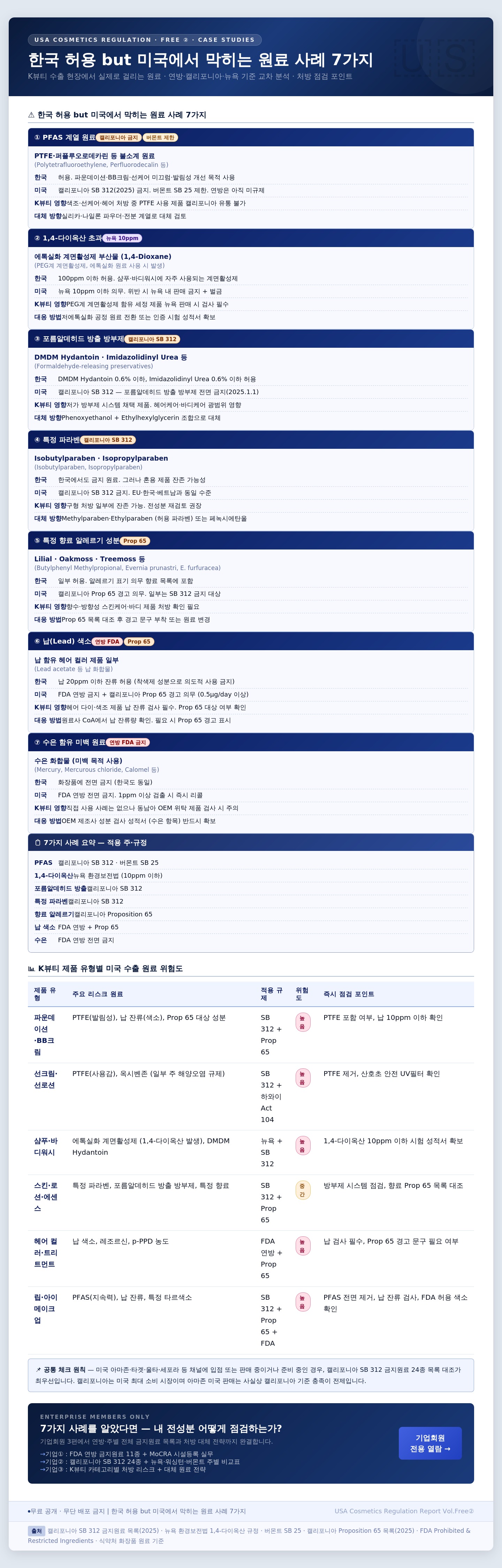
한국에서 아무 문제 없이 쓰던 원료가 미국 수출 시 걸리는 경우가 실제로 발생하고 있습니다. PTFE 같은 불소 계열 원료는 캘리포니아 SB 312로 2025년 1월부터 금지됐고, 샴푸·바디워시의 에톡실화 계면활성제 부산물인 1,4-다이옥산은 뉴욕 기준 10ppm 이하가 의무입니다. DMDM Hydantoin 같은 포름알데히드 방출 방부제도 캘리포니아에서 금지됐습니다. 이 자료는 K뷰티 처방에서 자주 사용하는 원료 중 미국에서 실제로 걸리는 7가지 사례를 원인·영향 제품·처방 대체 방향 세 축으로 정리했습니다.
기업① — FDA 연방 금지원료 11종 + MoCRA 시설등록 실무
연방 FDA 금지원료 11종 전체 목록과 각 금지 근거, K뷰티 관련성을 정리했습니다. MoCRA 시설등록은 2024년 7월부터 의무화됐습니다. 한국 제조사가 직접 등록할 수 없고 미국 대리인을 지정해야 하며, 2년마다 갱신이 필요합니다. 이 자료는 시설등록 5단계 프로세스, 국내 제조사와 해외 제조사의 의무사항 비교, 중대 이상반응 보고 체계, MoCRA 라벨링 기준을 실무 관점에서 정리했습니다.
기업② — 미국 주별 금지원료 완전 정리
캘리포니아 SB 312 금지원료 24종 전체 목록, 뉴욕·워싱턴·버몬트 4개 주의 규제 내용을 상세 정리했습니다. 각 주별로 어떤 원료가 금지·제한되는지, K뷰티 처방에서 어떤 영향을 받는지를 원료별 주별 교차 비교표로 제시합니다. 실무 핵심 원칙은 하나입니다. 캘리포니아 기준을 충족하면 연방과 다른 주 기준도 대부분 충족됩니다. 미국 수출 처방은 캘리포니아 기준으로 설계하는 것이 가장 효율적입니다.
기업③ — K뷰티 카테고리별 미국 수출 리스크 처방 가이드
스킨케어·선케어·색조·헤어·바디 제품 유형별로 어떤 원료가 어떤 규제에 걸리는지, 처방을 어떻게 바꿔야 하는지를 카테고리별로 정리했습니다. 단순히 금지 원료를 나열하는 것이 아니라 대체 원료와 처방 설계 전략까지 담았습니다. 마지막은 원료·처방 점검 8개 항목과 등록·라벨 점검 8개 항목으로 구성된 수출 전 자가진단 체크리스트로 마무리됩니다.
더 많은 정보를 원하신다면 아래 네이버 프리미엄 콘텐츠를 이용하세요.
와이에스엠경영컨설팅 윤수만